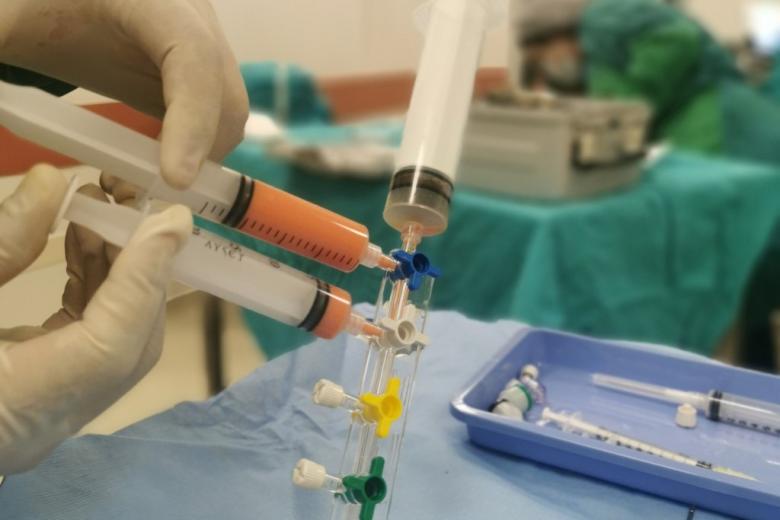
Eksperymenty medyczne z wykorzystaniem komórek macierzystych. RPO bada sprawę. Odpowiedź kliniki
- Media donoszą o kolejnych komercyjnych eksperymentach medycznych z wykorzystaniem komórek macierzystych, po których część pacjentów miała doznać uszczerbku na zdrowiu
- To ponowny przyczynek do dyskusji nad bezpieczeństwem takich badań, sposobem ich reklamowania i oferowania pacjentom oraz etycznością pobierania opłat za udział w nich
- Ważne rekomendacje przedstawił Zespół ekspertów Naczelnej Rady Lekarskiej ds. terapii komórkowych i komórek macierzystych
- AKTUALIZACJA: Eksperyment otrzymał pozytywną opinię Komisji Bioetycznej przy Okręgowej Izbie Lekarskiej w Warszawie, w momencie jego rozpoczęcia nie istniał prawny obowiązek ubezpieczenia, a relacja medialna o sprawie nie jest rzetelna - odpowiada radca prawny kliniki, w której dokonano eksperymentu
Rzecznik praw obywatelskich Marcin Wiącek prosi ministra zdrowia Adama Niedzielskiego o stanowisko. RPO pyta też o sprawę klinikę, która prowadziła eksperymenty, oraz prokuraturę.
RPO monitoruje kwestię wykonywania eksperymentów leczniczych z wykorzystaniem komórek macierzystych, oferowanych pacjentom za opłatą.
W związku ze skargami Rzecznik prowadził wcześniej w takiej sprawie korespondencję z Departamentem Kwalifikacji Medycznych i Nauki MZ. Zgłaszał wątpliwości wobec zgodności z kryteriami ustawowymi niektórych eksperymentów prowadzonych na ludziach z wykorzystaniem komórek macierzystych. Chodziło zwłaszcza o wątpliwości co do zgodności z aktualnym stanem wiedzy i zasadami etyki lekarskiej. Podnosił też kwestię opłat od pacjentów za udział w nich.
Dostał odpowiedź, że w ocenie MZ obecnie nie ma jednoznacznych i w pełni przekonujących dowodów na skuteczność terapii chorób mięśni za pomocą komórek macierzystych. Wskazano, że odpłatność udziału pacjenta w terapii eksperymentalnej komórkami macierzystymi, wobec czego lokalna komisja bioetyczna wyraziła pozytywną opinię, może budzić kontrowersje etyczne (ze względu na angażowanie środków finansowych pacjenta przy braku mocnych dowodów na skuteczność terapii). Ministerstwo informowało wówczas o planach wprowadzenia ustawowego zakazu pobierania opłat od uczestników.
Rzecznik zasięgnął także opinii Naczelnej Rady Lekarskiej. Wskazała ona m.in., że przyjęcie proponowanych przez MZ rozwiązań co do odpłatności powinno doprowadzić do wstrzymania nieuczciwych i naukowo wątpliwych eksperymentów. Jednocześnie stwarzałoby to jednak groźbę zablokowania realizacji wartościowych i uzasadnionych badań naukowych oraz terapii eksperymentalnych, które nie znajdą sponsora. Ostatecznie postulowane przez MZ rozwiązania nie zostały przyjęte.
Kwestie te pozostają problematyczne także obecnie. Ostatnio media podały bowiem informacje o klinice, w której prowadzono eksperyment medyczny z wykorzystaniem komórek macierzystych, w wyniku którego część pacjentów miała doznać uszczerbku na zdrowiu. Sprawa ta stała się kolejnym przyczynkiem do dyskusji nad bezpieczeństwem tego rodzaju badań, sposobem ich reklamowania i oferowania pacjentom oraz etycznością pobierania opłat za udział.
W marcu 2022 r. głos w sprawie komercyjnego oferowania zabiegów z wykorzystaniem komórek określanych jako macierzyste, w tym prowadzonych w ramach medycznych eksperymentów leczniczych, zabrał Zespół ekspertów Naczelnej Rady Lekarskiej ds. terapii komórkowych i komórek macierzystych.
Zwrócił on uwagę zwłaszcza na skutki uboczne zabiegów niepotwierdzonych rzetelnymi badaniami przedklinicznymi i klinicznym, określanych często jako „terapie z wykorzystaniem komórek macierzystych". Zespół podkreślił także, że udział pacjentów w terapiach, które są prezentowane jako panaceum, naraża ich na olbrzymie koszty. Zdaniem Zespołu, prowadzenie tego rodzaju terapii może także podważać zaufanie społeczne do medycyny i nauki, w tym do innowacyjnych metod leczniczych.
W ocenie Zespołu odpowiedzią na problem może być wdrożenie proponowanych rekomendacji. Część z nich wymaga podjęcia działań legislacyjnych. Dla realizacji innych wystarczy sumienne egzekwowanie obowiązujących już przepisów.
Zespół w szczególności postuluje:
- zasięganie przez Komisje Bioetyczne opinii niezależnych ekspertów posiadających wiedzę biologiczną, medyczną oraz doświadczenie w zakresie terapii komórkowych pozwalających na ocenę zasadności wniosków o przeprowadzenie eksperymentów leczniczych z wykorzystaniem HE-ATMP w określonych precyzyjnie wskazaniach;
- wprowadzenie regulacji prawnych ograniczających masowy i długotrwały charakter prowadzenia eksperymentów w ramach „wyjątku szpitalnego", w tym dążących do ograniczenia jego odpłatności;
- opracowanie zasad rzetelnego, merytorycznego informowania o terapiach komórkowych i egzekwowanie przepisów ustawy prawo farmaceutyczne w celu zapobieżenia nieuprawnionej promocji i reklamie zabiegów o niepotwierdzonej skuteczności HE-ATMP;
- przeprowadzenie analizy prawnej umów przedstawianych pacjentom pod kątem pełnego zabezpieczenia praw pacjentów na wypadek wystąpienia bezpośrednich i odległych działań niepożądanych, w tym stworzenie formularza świadomej zgody pacjenta i niedopuszczanie dokumentów umów z klauzulą całkowitej rezygnacji z roszczeń;
- podjęcie działań organizacyjnych i legislacyjnych w celu wprowadzenia obowiązku prawnego zgłaszania efektów ubocznych w przypadku HE-ATMP, a docelowo stworzenia rejestru zabiegów z obszaru eksperymentalnych terapii komórkowych w celu weryfikacji ich skuteczności i bezpieczeństwa.
Rzecznik prosi ministra o stanowisko w sprawie, zwłaszcza o odniesienie się do tych postulatów zmian, w tym prawnych.
Ponadto Biuro RPO zwróciło się do kliniki, w której doszło do eksperymentu. Zdaniem mediów niektórzy pacjenci mieli być utrzymywani w przekonaniu, że zabieg jest bezpieczny i nieinwazyjny; mieli też nie wiedzieć o ewentualnych skutkach ubocznych terapii. Jednocześnie mieli być informowani, że terapia eksperymentalna nie jest ubezpieczona.
Stąd prośba o podanie, w jaki sposób klinika wywiązała się z obowiązku informacyjnego względem pacjentów oraz z wynikającego z art. 23c ust. 1 ustawy o zawodach lekarza i lekarza dentysty obowiązku w zakresie ubezpieczenia.
Według mediów trwa śledztwo w tej sprawie. Dlatego Biuro RPO wystąpiło także do prokuratury o informacje na temat stanu postępowania.
Odpowiedź Moniki Zboralskiej, radcy prawnego Przychodni i Szpitala Okulistycznego Retina
Działając w imieniu mojego Mocodawcy, pełnomocnictwo w załączeniu, w odpowiedzi na pismo z dnia 13.10.2022 r. VII.5002.4.2022.AMB uprzejmie informuję, co następuje.
Eksperyment medyczny w Przychodni i Szpitalu Okulistycznym Retina był przeprowadzany przy spełnieniu wszystkich wymogów prawnych. Eksperyment otrzymał pozytywną opinię Komisji Bioetycznej przy Okręgowej Izbie Lekarskiej w Warszawie (dalej: „Komisja Bioetyczna”) pod przewodnictwem dr hab. n med. Marka Czarkowskiego. (Uchwała numer KB/1017/15 z dnia 19 listopada 2015r., w załączeniu).
Komisja Bioetyczna jest jedynym organem uprawnionym do akceptacji eksperymentu medycznego. W skład organu wchodzą specjaliści powołani do oceny eksperymentów medycznych, nie tylko w zakresie aspektów naukowych, ale także etycznych.
Komisja Bioetyczna, zatwierdziła wśród innych dokumentów formularze świadomej zgody i informacji dla pacjenta, a także sposób podawania preparatu.
Zgodnie z art. 29 ust. 22 pkt 3 i 4 ustawy o zawodzie lekarza i lekarza dentysty Postępowanie w sprawie wydania opinii jest wszczynane na wniosek, który zawiera (...)
• wzór informacji przeznaczonej dla uczestnika, zawierającej dane, o których mowa w art. 24 ust. 2;
• wzór formularza zgody uczestnika, w którym powinny być zawarte co najmniej stwierdzenia dotyczące:
• dobrowolnego wyrażenia zgody na poddanie się eksperymentowi medycznemu po zapoznaniu się z informacją, o której mowa w art. 24 ust. 2,
• potwierdzenia możliwości zadawania pytań prowadzącemu eksperyment medyczny i otrzymania odpowiedzi na te pytania,
• uzyskania informacji o możliwości odstąpienia od udziału w eksperymencie medycznym w każdym jego stadium.
Zgodnie z Obwieszczeniem Przewodniczącego Okręgowej Rady Lekarskiej w Warszawie z dnia 26 czerwca 2009 r w sprawie ogłoszenia tekstu jednolitego Regulaminu Komisji Bioetycznej przy Okręgowej Izbie Lekarskiej w Warszawie Załącznik nr 4 Komisja bada (.):
• czy informacja przekazywana uczestnikom eksperymentu, ich krewnym, opiekunom, prawnym opiekunom jest odpowiednia pełna i zrozumiała,
• jaka jest treść formularza świadomej zgody pacjenta (...).”
Dokumenty Świadomej zgody oraz Informację dla Pacjenta Komisja Bioetyczna szczególnie wnikliwie badała i dwukrotnie prosiła o zmianę dokumentu przed akceptacją.
W Uchwale Komisji Bioetycznej nr 50/15 z dnia 19.11.205 r. Komisja wydała pozytywna opinie o eksperymencie przy przyjęciu Zastrzeżenia (m. inn.): Badanie może zostać rozpoczęte pod warunkiem umieszczenia w Informacji dla Uczestnika Badania adnotacji na temat tego, ze powyższy eksperyment medyczny nie jest ubezpieczony, w związku z tym uczestnikowi badania nie przysługuje odszkodowanie, a w przypadku, kiedy doszło do wystąpienia szkód zdrowotnych związanych z podaniem komórek macierzystych może on wystąpić o odszkodowanie z indywidualnym roszczeniem na drodze sadowej.
W momencie rozpoczęcia eksperymentu nie istniał prawny obowiązku ubezpieczenia. Obowiązek ten został wprowadzony ustawą z dnia 16 lipca 2020 r. o zmianie ustawy o zawodach lekarza i lekarza dentysty oraz niektórych innych ustaw, czyli 4 lata po rozpoczęciu eksperymentu. Mój mocodawca starał się znaleźć ubezpieczyciela, gdyż również dla prowadzącego badania zwiększa to profil bezpieczeństwa. Niestety nikt na rynku nie chciał się podjąć ubezpieczenia. Z tego też względu komisja bioetyczna wnosiła o umieszczenie informacji w dokumentacji przekazywanej uczestnikom, iż eksperyment jest nieubezpieczony.
Pismem z dnia 20.07.2017r. Z/15377/1017/15 Komisja Bioetyczna poinformowała, iż na posiedzeniu w dniu 20.07.2017 r. zapoznała się i zaakceptowała prośbę o rozszerzenie grupy badanej oraz miedzy innymi Formularz Świadomej Zgody Pacjenta.
Jak widać, Komisji Bioetyczna kilkukrotnie zapoznawała się z dokumentacją przedstawianą pacjentowi i stwierdziła jej kompletność i prawidłowość. Tym samym nie można mówić, iż pacjenci nie byli prawidłowo informowani. Ponadto otrzymywali dokumenty wiele dni przed zabiegiem, aby mogli się z nimi zapoznać. Mogli zadawać pytania i byli dogłębnie informowani.
Z całą stanowczością pragnę też podnieść, iż program radiowy pn. „Eksperyment” w Tokfm nie spełnia podstawowych gwarancji rzetelnego i wiarygodnego dziennikarstwa, o wysokich standardach merytorycznych i etycznych. Na antenie została przedstawiona całkowicie jednostronnie, w sensacyjnym tonie historia jednego uczestnika, do tego relacjonowana przez osobę trzecią. Po audycji głos zabierali pacjenci, którzy brali udział w eksperymencie i wyrażali swoje oburzenie tonem i sensacyjnością audycji.
Pragnę również poinformować, iż Prokuratura Okręgowa w Warszawie po raz drugi umorzyła postepowanie w sprawie dotyczącej miedzy innymi pacjenta będącego bohaterem audycji. Dotychczasowa sygnatura akt to: PoV 22 2020. Ponieważ mój Mocodawca nie jest stroną w sprawie, nie ma dostępu do akt prokuratorskich i nie posiada postanowienia.
VII.5002.4.2022